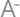 |
|
 |
|

图说:全国政协委员、上海市儿科医学研究所所长、上海交通大学医学院教授蔡威 来源/采访对象供图
目前,我国罕见病患者约有2000万人,每年新增患者超过20万人。临床工作者却面临患者能诊断但无相关产品或国外有但国内没有的困惑。全国政协委员、上海市儿科医学研究所所长、上海交通大学医学院教授蔡威建议加速罕见病特殊医学用途配方食品落地转化。
基于罕见病类特殊医学用途配方食品(以下简称“特医食品”)具有临床营养治疗、持续终生、无法被“普通肠内营养制剂”替代等特点,临床应用需求较为迫切,患者及家属呼声较高。在我国《第一、第二批罕见病目录》共207种中,有32种罕见病需使用特医食品,其中18种罕见病对特医食品的需求尤为紧急与重要,但目前国内到2024年2月已经批准注册证书的特医食品有179种,但仅有针对苯丙酮尿症不同年龄段患者的3款进口特医食品获得产品注册证书。
“国家市场监督管理总局高度重视罕见病类特医食品注册审批问题,近年来多次对上海等省市相关医疗机构实地调研,了解苯丙酮尿症等多种罕见病的特医食品临床使用需求,探索构建罕见病特医食品应急审评机制,保障罕见病患者特医食品供应。” 蔡威委员说:“2023年12月出台了优化罕见病类特医食品注册审批制度,这对罕见病患者是个福音,但具体落地转化为可及的产品还存在不少困难。”
因此,他建议进一步放宽罕见病类特医食品注册审批制度,对成熟的进口产品实行先有条件注册许可进口和临床使用,同时要求企业和临床医师使用中实时收集数据上报,以利统计汇总观察相关产品的安全性和有效性,为正式是否通过注册发证提供科学数据。同时,建议针对国内自主产品短缺,建立专门绿色通道,实行单独“排队”或优先审评,对前期工作扎实、可靠、科学的产品也可实施有条件批准、上市后临床效果跟踪评估及退出机制。此外,对从事罕见病产品研发的企业予以一定的财政政策支持,使企业既能承担社会义务,又能微利可图,这样有利企业可持续高质量发展。
新民报系成员|客户端|官方微博|微信矩阵|新民网|广告刊例|战略合作伙伴
北大方正|上海音乐厅|中卫普信|今日头条|钱报网|中国网信网|中国禁毒网
增值电信业务经营许可证(ICP):沪B2-20110022号|互联网新闻信息服务许可证:31120170003|信息网络传播视听节目许可证:0909381
广电节目制作经营许可证:(沪)字第536号|违法与不良信息举报电话15900430043|跟帖评论自律管理承诺书
 |沪公网安备 31010602000044号|沪公网安备 31010602000590号|沪公网安备 31010602000579号
|沪公网安备 31010602000044号|沪公网安备 31010602000590号|沪公网安备 31010602000579号
新民晚报官方网站 xinmin.cn ©2024 All rights reserved